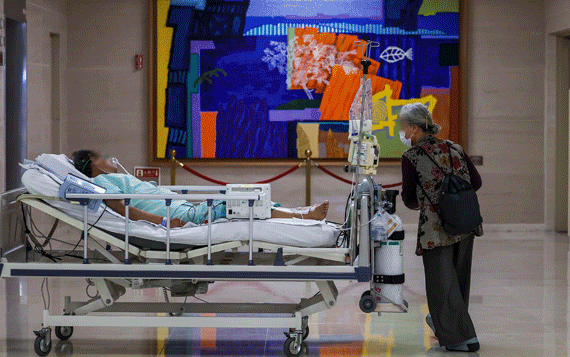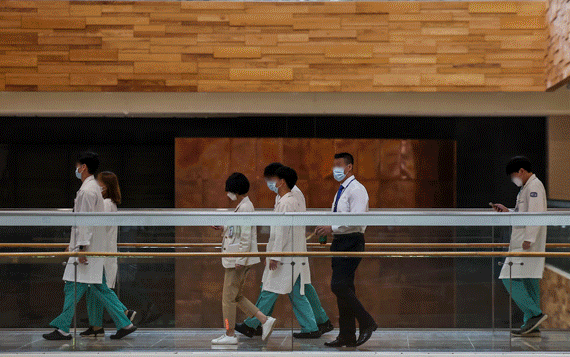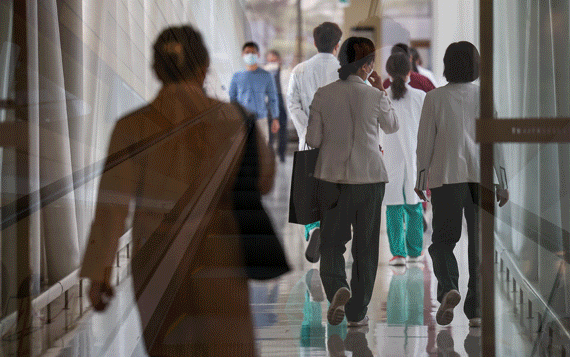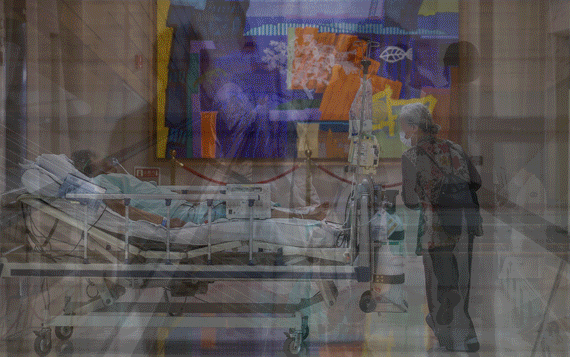인보사 행정소송 본격화… 코오롱생명과학, 식약처에 제소
허가취소 효력정지신청

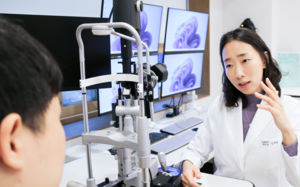
【서울=뉴시스】박미소 기자 = 이우석 코오롱생명과학 대표가 4일 오전 서울 중구 프레스센터에서 열린 '투약 환자 안전관리 종합 대책(안) 발표 기자회견'에 앞서 사과문을 발표하고 있다. 2019.07.04. [email protected]
【서울=뉴시스】송연주 기자 = 골관절염 유전자 치료제 ‘인보사케이주’ 허가 취소를 둘러싼 식품의약품안전처와 코오롱생명과학의 소송이 본격화된다.
코오롱생명과학(대표 이우석)은 식약처의 인보사케이주 관련 행정처분에 대한 취소청구 소장과 효력정지신청서를 서울행정법원 및 대전지방법원에 제출했다고 9일 공시했다.
코오롱이 행정소송을 제기한 처분은 ▲인보사케이주 품목허가 취소 처분 ▲인보사케이주 임상시험 계획승인 취소처분 ▲인보사케이주 의약품 회수·폐기 명령 등이다.
앞서 식약처는 지난 3일 뒤바뀐 세포 파문으로 인보사의 품목허가를 취소했고, 코오롱생명과학은 처분에 대한 불복 의사를 밝힌 바 있다.
코오롱생명과학은 “청문절차에서 인보사의 안전성과 유효성, 착오로 인해 당사가 제출한 품목허가신청 서류에 인보사 2액의 성분유래에 대한 기재가 사실과 달랐으나 고의적인 조작이나 은폐는 결코 없었다는 점을 충분히 소명했음에도 식약처가 품목허가취소를 결정한 것에 대해 유감스럽다”고 밝혔다.
이어 “행정소송의 제기를 통해 식약처의 품목허가취소처분이 과연 적법한지에 대한 법원의 판단을 구할 것이고, 인보사를 필요로 하는 환자분들께 다시 제공할 수 있게 되기를 희망한다”고 강조했다.
법적 대응의 이유로는 ▲식약처가 주관한 모든 임상시험을 동일한 세포로 진행해 안전성의 우려가 없고 ▲고의적 은폐는 사실이 아니며 ▲GP2 293세포의 종양 유발 가능성에 대한 과학적 검증 확인 과정 필요 등을 꼽았다.
◇환자·주주·보험사와 소송 직면
코오롱생명과학은 식약처와의 행정소송 외에 환자 및 주주, 보험사와의 행정소송에 직면하고 있다. 손해보험사들도 보험금으로 부당 지급된 인보사 판매대금을 돌려달라며 소송에 나섰다.
특히 손해배상청구 소송 참여 환자는 현재까지 767명에 이른다. 지난 5월28일 244명의 손해배상청구 소장이 접수된 이후, 6월1일부터 28일까지 2차 모집기간 동안 총 523명의 피해환자가 소송 참여 의사를 밝히며 위임장 등 관련 서류 제출을 완료했다. 1~2차 모두 합하면 767명이다.
소송 대리인인 법무법인 오킴스는 “환자들은 대부분 중등도 이상의 고령자들이어서 종양 유발 가능성 있는 세포가 신체에 주입된 사실 만으로 극도의 불안을 느낀다”며 “또 세포가 바뀌었다는 사실을 알았더라면 인보사를 투약받기로 결정하지 않았을 것이라는 점에서 환자들의 자기결정권을 심대하게 침해받았다”고 제소 이유를 설명했다.
[email protected]
Copyright © NEWSIS.COM, 무단 전재 및 재배포 금지