미코바이오메드, 원숭이두창 진단키트 수출허가 획득
아프리카에 원숭이두창 진단키트 공급 추진
美 FDA에 긴급사용승인 신청 예정

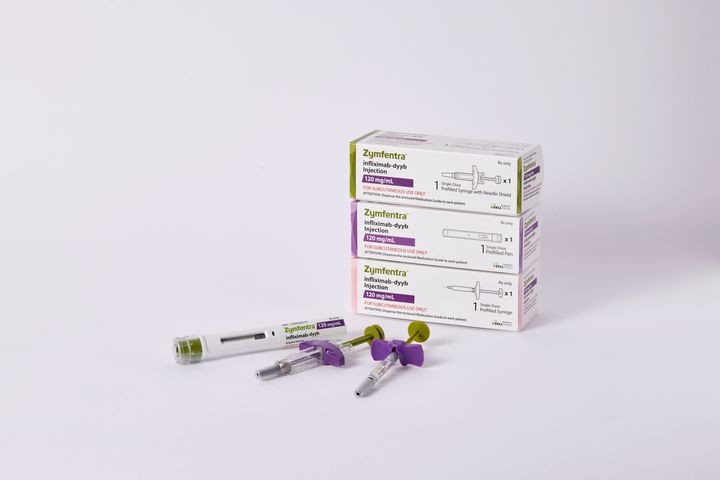
[서울=뉴시스] 안호균 기자 = 체외진단의료기기 제조사 미코바이오메드가 국내 최초로 원숭이두창 PCR 진단키트(Veri-Q MCMPx-VS)의 식품의약품안전처 수출허가를 획득했다고 21일 밝혔다.
미코바이오메드가 수출허가를 받은 제품은 2016년 질병관리청의 연구용역과제 수행을 통해 개발을 완료하고 공동 특허를 등록한 원숭이두창 진단키트다.
회사는 지난 7월 세네갈 파스퇴르 연구소에서 원숭이두창 진단키트의 임상시험을 진행했다. 그 결과 민감도(양성 확인율)와 특이도(음성 확인율) 모두 100%의 결과를 얻어 성능을 입증했다.
회사는 우선 이번 임상시험에 협조한 세네갈 파스퇴르 연구소를 통해 아프리카 지역에 원숭이두창 바이러스 키트를 공급하는 것을 추진 중이다.
회사 관계자는 "이번 임상시험에 협조한 세네갈 파스퇴르 연구소는 서아프리카 지역에서 감염병 예방과 진단, 치료의 컨트롤 타워 기능을 수행하고 있는 기관"이라며 "해당 기관과의 협업을 통해 감염병혁신연합(CEPI) 등의 국제 보건협력기구에 원숭이두창 바이러스 진단키트를 공급해 아프리카 지역을 공략할 계획"이라고 말했다.
감염병혁신연합(CEPI)은 2017년에 빌&멜린다 게이츠 재단과 각국의 자선기금을 통해 창설된 감염병 백신 개발을 지원하는 국제 민간기구다.
미국 시장 진출도 추진한다.
회사 측은 "이달 7일 미국 보건복지부가 원숭이두창 진단키트에 대한 긴급사용승인(EUA) 도입을 발표했다"며 "미국 자회사 미코바이오메드 USA의 적극적인 협조를 통해 신속히 미 식품의약국(FDA)에 EUA를 신청할 예정"이라고 전했다.
◎공감언론 뉴시스 [email protected]
Copyright © NEWSIS.COM, 무단 전재 및 재배포 금지