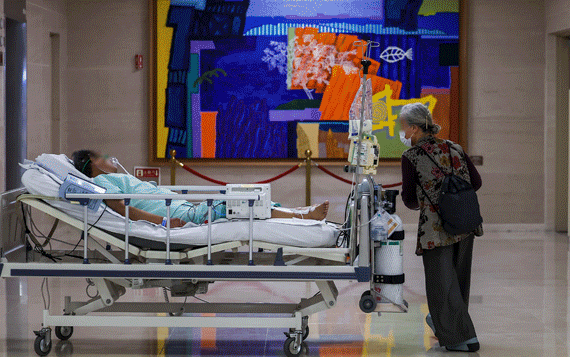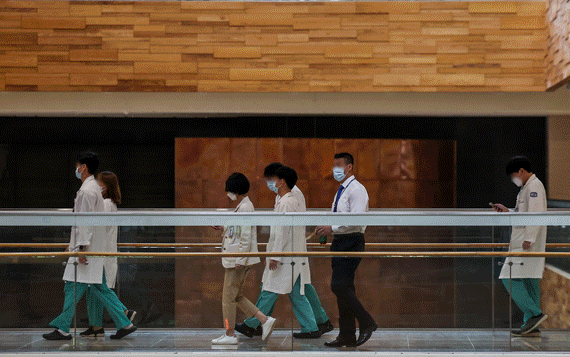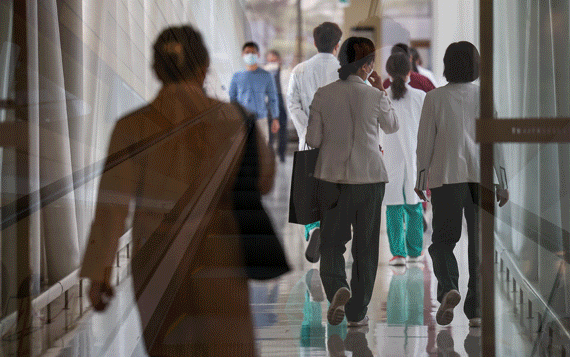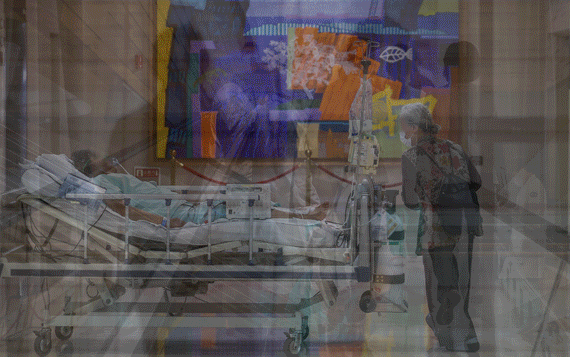유럽, 인도 100개 제네릭의약품 사용중단 권고…품질 우려
생물학적 동등성 연구 자료, 신뢰성 우려

【서울=뉴시스】황재희 기자 = 유럽의약품청(EMA)이 최근 인도의 CRO(임상시험수탁기관) 기업인 싱크론 리서치 서비스(Synchron Research Services)에서 수행한 100개 제네릭(복제약) 제품에 대해 사용중단을 권고했다.
27일 한국바이오협회에 따르면, 지난 20일 EMA는 싱크론이 수행한 생물학적 동등성 연구에서 불규칙성이 발견됐고, 이것이 복제약 품질관리시스템과 데이터 신뢰성에 심각한 우려가 제기된다며 제네릭 사용 중단을 권고했다.
앞서 싱크론은 작년 9월에도 미국 식품의약국(FDA)으로부터 데이터 무결성 우려로 실사를 받은 바 있다. FDA는 싱크론에서 수행한 임상 및 생물학적 분석 결과로 신약이나 제네릭 허가신청을 불허한다는 내용을 기업들에게 공지한 바 있다.
또 2019년에는 싱크론이 데이터 분석방법 훼손 행위 및 과정 등으로 위조된 연구데이터를 제출해 비난을 받은 바 있다.
한국바이오협회 바이오경제연구센터는 “EMA는 이로 인해 영향을 받은 약 100개의 제네릭의약품은 다른 곳에서 적절한 생물학적 동등성 자료가 없어 중단이 권고되지만, 다른 의약품으로 대체할 수 없는 경우 중단을 일시적으로 연기할 수 있다고 했다”며 “유럽 국가들은 의약품 회수가 자국에서 필요한지 여부를 결정해야 한다”고 말했다.
이에 따라 글로벌 제약사인 존슨앤드존슨(J&J)과 산도스, 테바, 비아트리스 등을 포함해 인도 의약품제조회사 워크하트 등이 영향을 받게 됐으며, 인도 CRO기업에 대한 신뢰도 역시 또 한 번 타격을 입을 것으로 전망된다.
바이오경제연구센터 관계자는 “문제가 된 인도 CRO는 인도에서 데이터 조사를 받은 최초의 기업이 아니다”라며 “FDA와 EMA는 이전에도 세믈러 리서치, GVK 바이오사이언스 등 인도 CRO기업에 유사한 문제를 제기한 바 있다”고 했다.
◎공감언론 뉴시스 [email protected]
Copyright © NEWSIS.COM, 무단 전재 및 재배포 금지