온코닉 "식약처, 항암신약후보 임상 1상 계획변경 승인"
음식물 영향 및 인종 간 차이 평가
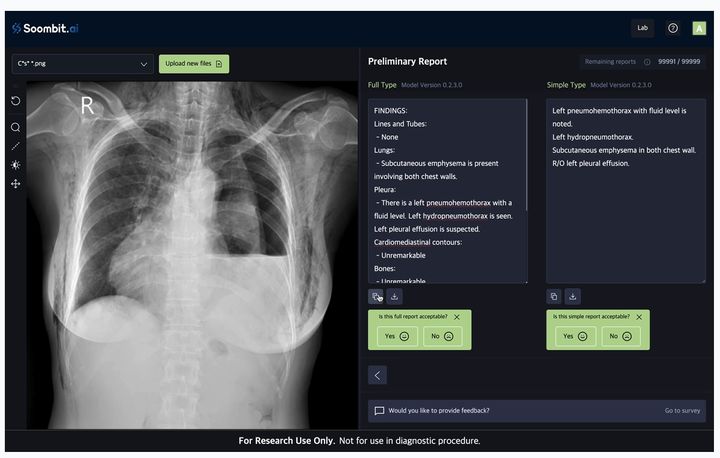
![[서울=뉴시스] 온코닉테라퓨틱스가 식품의약품안전처로부터 이중표적 합성치사 항암신약후보 '네수파립'의 음식물 영향 및 인종 간 차이를 평가하기 위한 임상시험 1상 계획 변경을 승인받았다고 공시를 통해 9일 밝혔다. (사진=온코닉테라퓨틱스 제공) 2026.03.09. photo@newsis.com](https://img1.newsis.com/2026/02/24/NISI20260224_0002068662_web.jpg?rnd=20260224093407)
[서울=뉴시스] 온코닉테라퓨틱스가 식품의약품안전처로부터 이중표적 합성치사 항암신약후보 '네수파립'의 음식물 영향 및 인종 간 차이를 평가하기 위한 임상시험 1상 계획 변경을 승인받았다고 공시를 통해 9일 밝혔다. (사진=온코닉테라퓨틱스 제공) 2026.03.09. [email protected]
네수파립은 PARP와 탄키라제(TNKS)를 동시에 저해하는 이중기전 합성치사 항암제로 기존 PARP 저해제와 차별화된 이중표적항암 신약후보물질이다.
이번 임상시험 1상은 건강한 한국인, 코카시안 및 중국인 성인 남성을 대상으로 음식물 또는 인종 간 차이가 네수파립 경구 투여 시 미치는 약동학적 특성과 안전성·내약성을 평가하기 위한 목적을 지닌다.
글로벌 개발과 허가를 위해 식이 영향 및 인종 간 약동학(PK) 차이를 살피기 위한 별도의 임상 1상이다.
이번 임상은 무작위 배정, 공개, 단회 투여, 교차설계 방식이며 서울대병원에서 진행된다. 임상시험 기간은 의학연구심사위원회 승인일로부터 약 12개월이다. 회사는 목표 시험대상자 수를 36명으로 예상했다.
온코닉테라퓨틱스는 임상 1상 예상종료일을 내년 3월 9일로 지정했다. 회사는 해당 예상종료일은 임상시험 계획신청서상 시험기간 예상종료일이며, 추후 변동될 수 있다고 설명했다.
또 기존 승인을 받은 자궁내막암, 췌장암, 위암 및 난소암의 임상2상 또는 임상 1b·2상은 계획대로 진행 중이라고 덧붙였다.
◎공감언론 뉴시스 [email protected]
Copyright © NEWSIS.COM, 무단 전재 및 재배포 금지