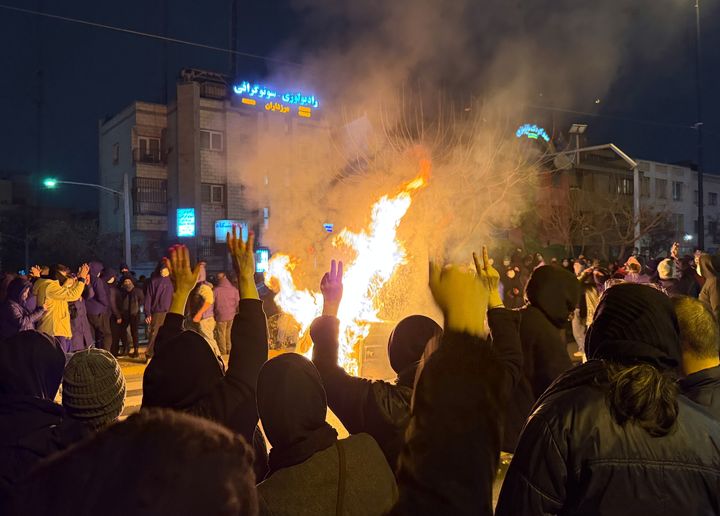"처음부터 끝까지 규제대응"…식약처 올해도 '이것' 운영
식약처, '국가 R&D 규제정합성 검토제도' 운영
5월 22일까지 규제정합성 검토 수요조사 실시
희귀·난치 질환 치료제 등 신속한 제품화 기대
![[서울=뉴시스] 식품의약품안전는 식·의약 혁신제품 개발을 지원하기 위해 국가연구개발사업을 추진·수행하는 정부 부처 등을 대상으로 내달 22일까지 '국가 연구개발(R&D) 규제정합성 검토' 수요조사를 실시한다고 28일 밝혔다. (사진=뉴시스DB) 2024.01.10. photo@newsis.com *재판매 및 DB 금지](https://img1.newsis.com/2024/01/10/NISI20240110_0001456600_web.jpg?rnd=20240110164124)
[서울=뉴시스] 식품의약품안전는 식·의약 혁신제품 개발을 지원하기 위해 국가연구개발사업을 추진·수행하는 정부 부처 등을 대상으로 내달 22일까지 '국가 연구개발(R&D) 규제정합성 검토' 수요조사를 실시한다고 28일 밝혔다. (사진=뉴시스DB) 2024.01.10. [email protected] *재판매 및 DB 금지
[서울=뉴시스]송종호 기자 = 지난해 인공혈액 등 혁신제품에 대한 규제 요건 및 대응 전략 등 컨설팅을 제공해 높은 만족도를 기록했던 지원 사업이 올해도 이뤄진다.
식품의약품안전는 식·의약 혁신제품 개발을 지원하기 위해 국가연구개발사업을 추진·수행하는 정부 부처 등을 대상으로 내달 22일까지 '국가 연구개발(R&D) 규제정합성 검토' 수요조사를 실시한다고 28일 밝혔다.
규제정합성 검토 제도는 국가 R&D 식·의약 혁신 제품의 개발 초기단계부터 인·허가에 필요한 평가기준 방법, 요건 등을 진단해 ▲규제대응 전략을 제공하고 기존 규제로 포섭되지 않는 첨단·신개념 제품은 평가체계 마련을 위한 ▲공동 연구 필요성까지 검토함으로써 신속한 시장 진입을 돕는 제도이다. 검토 결과는 사전상담-임상승인-허가심사에 연계해 지원 받을 수 있도록 함으로써 제품화 시행착오를 줄여줄 것으로 기대된다
국가연구개발사업을 추진하는 중앙행정기관은 사업을 수행하는 연구자로부터 신청을 받는 경우 이를 식약처에 규제정합성 검토를 요청할 수 있다.
연구자는 규제정합성 검토 결과를 토대로 품목분류, 임상시험 및 품목허가 신청 등 향후 규제 대응계획을 미리 수립할 수 있으며, 식약처는 상담, 회의 등을 통한 질의응답 및 의견수렴의 기회도 폭넓게 마련해 궁금증과 애로사항을 적극 해소할 예정이다.
식약처는 "시범사업을 통해 인공혈액, 재생의료 치료제 등 국가 R&D 개발 5개 제품에 대한 규제 요건 및 대응 전략 등 컨설팅을 제공해 높은 만족도를 확인했다"라고 설명했다. 만족도는 100점 만점에 제도전반 93.8점, 운영절차·소통·제공정보 활용도 등 95.8점을 기록했다.
올해도 공중보건 위기대응 의료제품, 희귀·난치 질환 치료제, 신소재 식품 등 혁신제품 개발 국가 R&D에 대한 규제정합성 검토를 지원한다.
식약처는 "규제정합성 검토 제도가 국가 R&D 식·의약 혁신제품의 규제 예측성을 높이고 시행착오를 최소화하는데 도움이 될 것으로 기대한다"라며 "앞으로도 제도를 지속 운영하여 첨단·혁신 기술의 가치가 제품화를 통해 국민께 신속히 전달될 수 있도록 적극 지원할 계획이다"라고 밝혔다.
◎공감언론 뉴시스 [email protected]
Copyright © NEWSIS.COM, 무단 전재 및 재배포 금지